ベランタマブ マホドチン、眼障害の留意点を周知依頼
再発/難治性の多発性骨髄腫治療薬
厚生労働省医薬局医薬品審査管理課長、医薬局医薬安全対策課長は昨日(5月19日)付で連名通知(医薬薬審発0519第2号、医薬安発0519第1号)を発出。同日付で1ライン以上の治療歴を有する成人の再発/難治性の多発性骨髄腫の治療薬として製造販売承認を取得した抗BCMA抗体薬物複合体ベランタマブ マホドチン(商品名ブーレンレップ点滴静注用100mg)について、視力低下などの眼障害が高頻度に認められることから、留意事項の周知を依頼する事務連絡を通知した。(関連記事「再発/難治性多発性骨髄腫へのベランタマブ マホドチン併用療法が承認」)
休薬・減量・中止の基準を提示
ベランタマブ マホドチンは今回、ボルテゾミブ+デキサメタゾンまたはポマリドミド+デキサメタゾンとの併用療法として、再発/難治性の多発性骨髄腫に対する承認を取得した。同薬は視力低下などの眼障害が高頻度に認められており、点状表層角膜症などが現れ、角膜潰瘍など、重篤な眼障害に進行した症例も報告されている。主な留意事項は以下の通り(電子添付文書から抜粋)。
警告:①緊急時に十分対応できる医療施設において、造血器悪性腫瘍の治療に対して十分な知識・経験を持つ医師の下で、本剤の投与が適切と判断される症例のみに行う、②治療開始に先立ち、患者またはその家族に有効性および危険性を十分に説明し、同意を得てから投与を開始する、③眼科医との連携の下で使用し、本剤の投与開始前に眼科医による診察を実施する、④異常が認められた場合には投与を中止するなど適切な処置を行うとともに、眼科医による評価を行う-こと
用法および用量に関連する注意:①併用する抗悪性腫瘍薬の投与に際しては、「臨床成績」の項の内容を熟知し、投与する、②ボルテゾミブおよびデキサメタゾン併用投与の場合、併用投与終了後も本剤単独投与を継続する、③本剤の投与により副作用が発現した場合には、以下の基準を参考に、休薬・減量・中止する(表1~3)-こと
表1. 減量する場合の投与量
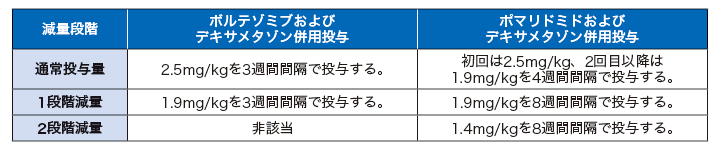
表2. 副作用に対する休薬・減量・中止基準
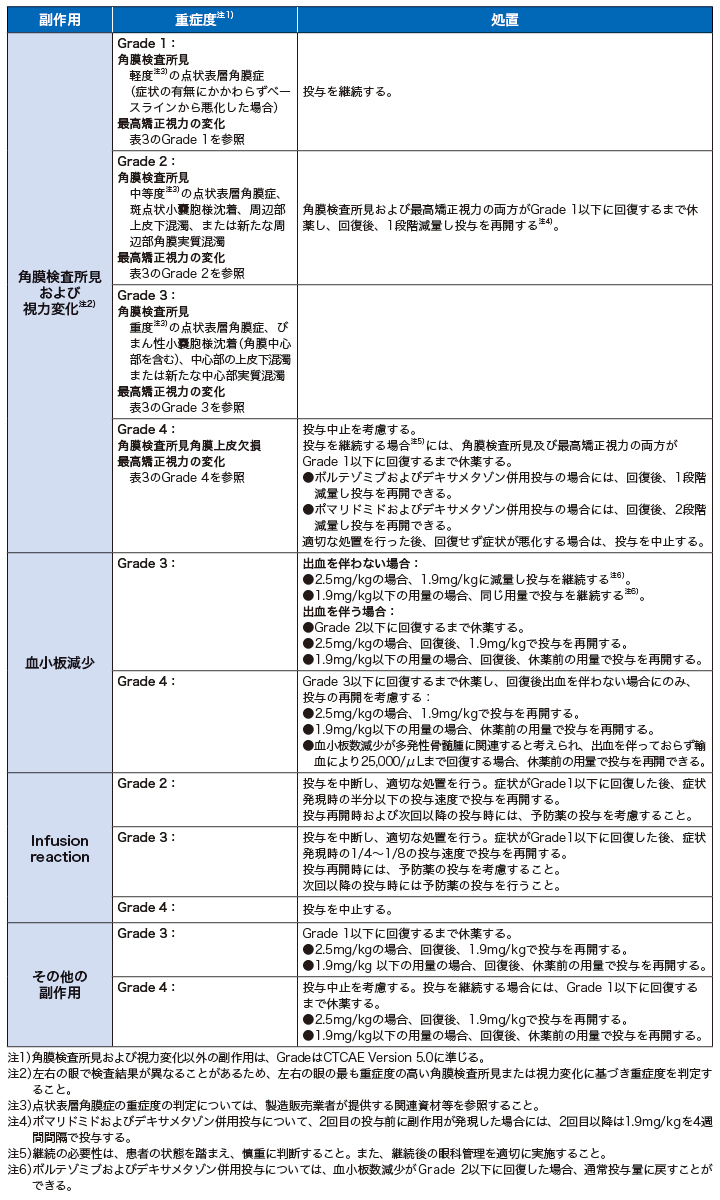
表3. 眼障害による最高矯正視力の変化の重症度
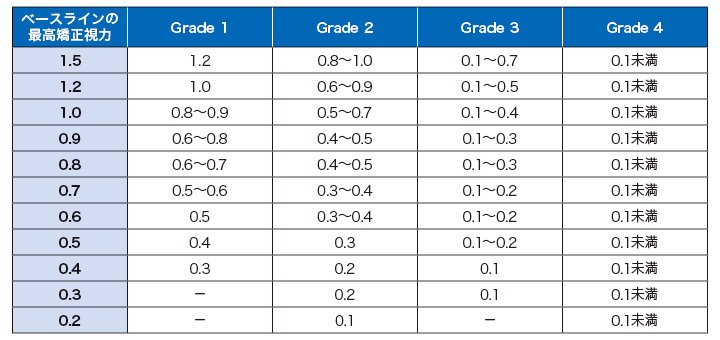
(表1~3とも厚生労働省2025年5月19日付事務連絡)
重要な基本的注意:眼障害が現れることがあるので、本剤の投与に当たっては、以下の事項に注意すること。①投与開始前に眼科医による診察を実施する、②初回から4回目までの各投与前は必ず、その後の投与期間中は必要に応じて、眼科医による視力検査および細隙灯顕微鏡検査を含む眼科検査を実施し、患者の状態を十分に観察する、③2回目の投与から休薬または減量を要する場合や、長期の休薬を要する場合があるため、「7. 用法及び用量に関連する注意」の項を参考に対処する、④眼の異常が認められた場合には、速やかに医療機関を受診するよう患者を指導し、眼科医による評価を行う、⑤ドライアイなどの眼症状を軽減するため、投与中は防腐剤を含まない人工涙液を1日4回以上投与するよう患者を指導する、⑥投与中はコンタクトレンズの装着を避けるよう患者を指導する、⑦視力低下につながる霧視などの眼障害が高頻度に認められているため、自動車の運転や機械の操作などを行う際に注意するよう患者を指導する-こと
特定の背景を有する患者に関する注意:①合併症・既往歴などがある、②角膜上皮疾患(軽度の点状角膜症を除く)を合併している、③眼障害の発現または増悪リスクが高まる恐れがある-患者。なお臨床試験において、当該患者は除外された
重大な副作用:①眼障害〔視力低下(90.2%)、角膜検査所見(角膜症など、86.6%)、霧視(69.2%)、羞明(43.8%)、視力障害(11.5%)、角膜潰瘍(1.2%)など〕が現れることがある。特に、角膜上皮欠損や角膜潰瘍(感染性角膜炎および潰瘍性角膜炎を含む)が疑われる眼症状が現れた場合には、速やかに患者を眼科に受診させ、適切な処置を行うこと
(編集部・関根雄人)
無料でいますぐ
会員登録を行う
- ご利用無料、14.5万人の医師が利用
- 医学・医療の最新ニュースを毎日お届け
- ギフト券に交換可能なポイントプログラム
- 独自の特集・連載、学会レポートなど充実のコンテンツ
\ 60秒でかんたん登録 /
会員登録












