実臨床を反映しない日本の「実臨床研究」
元凶は「レセプトデータベース」の致命的欠陥
国際的に広く認知されるRWE研究だが...
薬剤の有効性や安全性(ファーマコビジランス)に対する「実臨床研究(リアルワールドエビデンス研究:RWE研究)」が世界中で盛んに行われている。製薬メーカーによる従来の市販後調査(post marketing surveillance:PMS)に加えて、近年はアカデミア主体の「大規模コホート研究」と銘打った報告が増加している。その多くは診療報酬明細書(レセプト)情報(claims data)を中心としたデータベースの解析で、1990年代に欧米で始まり、現在では実臨床研究の主要な手段として国際的に広く認知されている(図)。
図. 世界のレセプトデータ研究の年次推移(PubMedで「claims database X cohort study」でヒットした論文数)
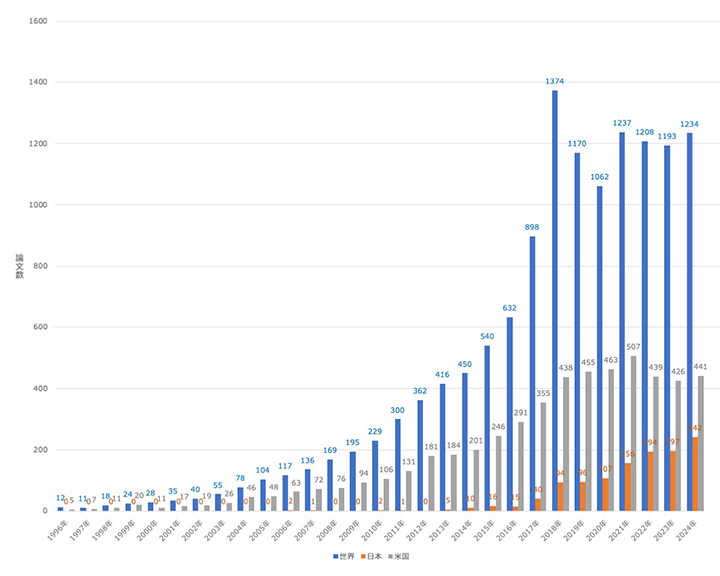
このレセプトデータベース(claims database)を用いた研究は2000年代には日本にも輸入された。当初は、医療費分析、有病率調査、製薬マーケティングなどの目的で利用されているにすぎなかったが、2010年前後から「レセプトデータは実臨床を反映している」ことを前提とした国内RWE研究が出現し、その後は国内でも増加を続けている。
しかしながら、日本におけるレセプトデータを用いたRWE研究の科学的信憑性は欧米に比べると極めて低い。日本と欧米ではレセプトそのものの内容に違いがあり、欧米と違って日本のレセプトデータは実臨床を反映しているとはとても言えないからである。
全文を読むにはログインが必要です
ログインして全文を読む
無料でいますぐ
会員登録を行う
- ご利用無料、14.5万人の医師が利用
- 医学・医療の最新ニュースを毎日お届け
- ギフト券に交換可能なポイントプログラム
- 独自の特集・連載、学会レポートなど充実のコンテンツ
\ 60秒でかんたん登録 /
会員登録












