一部ステロイド製品の効能・効果を削除
日本神経学会/ファイザー
日本神経学会は昨日(11月10日)、ファイザーが製造販売するヒドロコルチゾン(商品名コートリル錠10mg)、ヒドロコルチゾンコハク酸エステルナトリウム(ソル・コーテフ注射用100mg)、メチルプレドニゾロン酢酸エステル(デポ・メドロール水懸注20mg、同40mg)について、効能・効果の一部を削除することについて厚生労働省、関連学会の了承を取得し、電子化された添付文書(電子添文)を改訂したと発表した。(関連記事「ソル・コーテフの最新供給状況を案内」、「デポ・メドロールが限定出荷に」)
今回、削除の対象となる製品と効能・効果は以下の通り。
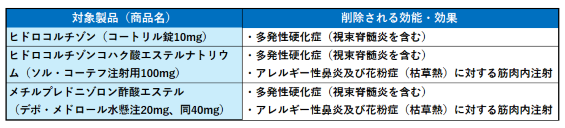
同社は削除の理由として、①多発性硬化症:米・ファイザー社において有効性と安全性について文献レビューおよびガイドラインの確認などを行った結果、多発性硬化症の急性増悪治療における使用を支持するデータは特定されなかった、②アレルギー性鼻炎および花粉症(枯草熱):米・ファイザー社において有効性と安全性について文献レビューおよびガイドラインの確認などを行った結果、「アレルギー性鼻炎」および「花粉症(枯草熱)」の筋肉内投与による使用については、現行の治療法と同等以上であることを支持するデータが不足しており、ガイドラインでは非経口コルチコステロイドは推奨されていないことが確認された。また、注射部位反応や過敏症などの全身性反応の発現リスクが、アレルギー性鼻炎に対する非経口コルチコステロイド投与のベネフィットを上回る可能性が示唆された-を挙げている。
無料でいますぐ
会員登録を行う
- ご利用無料、14.5万人の医師が利用
- 医学・医療の最新ニュースを毎日お届け
- ギフト券に交換可能なポイントプログラム
- 独自の特集・連載、学会レポートなど充実のコンテンツ
\ 60秒でかんたん登録 /
会員登録













