再生医療「日本ルール」の致命的欠陥
自家培養軟骨「ジャック」の「変形性膝関節症」への適応拡大を考える
初めに:手術・入院・リハビリ...患者負担の大きい治療
今年(2026年)1月、自家培養軟骨「ジャック」(J-TECと広島大学の共同開発)が再生医療等製品として「変形性膝関節症(knee osteoarthritis:膝OA)」に適応拡大・保険収載された(関連記事「変形性膝関節症、自家培養軟骨ジャックへの期待」)。
「ジャック」は、外来処置や処方で完結する治療ではない。まず、入院して関節鏡下での軟骨採取手術から始まる。膝関節内の健常部位(主に大腿骨顆部の非荷重部)から軟骨を切除し、これを原材料として細胞加工施設へ送付する。採取された軟骨細胞は、施設で数週間にわたり培養され、アテロコラーゲンゲルに包埋された「培養軟骨」として製品化される。製造工程では動物由来原料も使用されるため、事前の皮内テストやアレルギー評価が必須とされ、適応には複数の制約条件が課されている。
その後、2回目の手術として培養軟骨の移植術が行われる。変性した軟骨を除去した欠損部に培養軟骨を挿入し、さらにコラーゲン膜や骨膜を用いて縫合固定する。術後には移植片の脱落や肥大を防ぐため、荷重制限や可動域制限が課され、慎重な術後管理と約1カ月の段階的なリハビリテーションが不可欠となる(図)。
図. ジャックの治療プロトコール
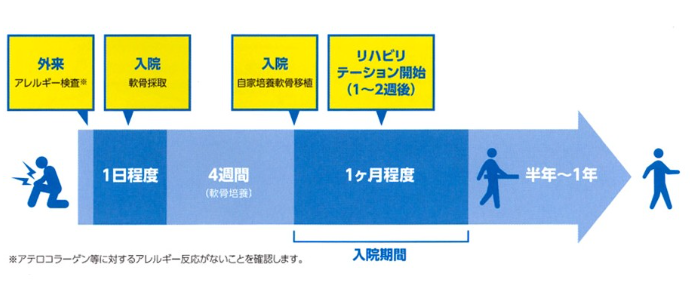
(川口 浩氏提供)
すなわち「ジャック」は、外来通院でのヒアルロン酸(HA)注射や薬物療法とは本質的に異なり、「2回の手術+入院+細胞加工+集中的リハビリ」という極めて長期で煩雑な医療プロセスを要する治療である。いうまでもなく、患者は大きな身体的・時間的・経済的・心理的負担を強いられることになる。
「ジャック」は2012年に、外傷性軟骨欠損症・離断性骨軟骨炎というマイナーな適応症に対して承認・保険収載されたが、今回、超メジャーな「膝OA」に適応拡大されて市場に出たことになる。適応症名は「膝OA」だが、その下に「効果・効能」として「膝OAに対する『臨床症状の改善』」と付記されている。さらに、「保存療法に反応せず、軟骨欠損面積が2cm²以上の症例に限る」、という条件付きである(添付文書)。
今回の適応拡大・保険収載の経緯を検証すると、日本の再生医療、ひいては日本の薬事・医療制度が抱える極めて特殊な構造的問題が露呈する。
全文を読むにはログインが必要です
ログインして全文を読む
無料でいますぐ
会員登録を行う
- ご利用無料、14.5万人の医師が利用
- 医学・医療の最新ニュースを毎日お届け
- ギフト券に交換可能なポイントプログラム
- 独自の特集・連載、学会レポートなど充実のコンテンツ
\ 60秒でかんたん登録 /
会員登録














